图1
依托咪酯作为一种酯类化合物,进入人体后主要在肝内降解,其主要代谢产物为依托咪酯酸(分子结构见图2),进一步水解生成乙醇和羧酸,并最终随尿液或胆汁排出[6-7]。研究[8]发现,静脉注射依托咪酯后1 d内,近75%的依托咪酯从尿液中排出,其中极少部分是以原形形式。此外,针对依托咪酯的检测,有研究[9-10]使用高效液相色谱法对血液中的依托咪酯进行检测,但该方法前处理操作繁琐,且灵敏度较低;有研究[11]使用高效液相色谱-串联质谱法(high performance liquid chromatography-tandem mass spectrome-try,HPLC-MS/MS)对尿液中的依托咪酯进行分析检测,尽管灵敏度较既往研究大幅提高,但该方法不仅对检材的利用率低,而且尿液样品仅通过超高速离心处理,对仪器性能要求较高。目前有关依托咪酯的检测多为原体检测,对代谢物涉及较少,如需推断给药时间,则要参考代谢物的实际情况[12-13]。因此,以依托咪酯和依托咪酯酸为目标物,能够有效满足对人体内依托咪酯的定性定量测定要求,同时,尿液样品相对于血液、组织等检材而言更容易获取且前处理更为简单[14]。
图2
本研究旨在建立一种尿液样品中依托咪酯和依托咪酯酸的HPLC-MS/MS检测方法,并应用于实际案例,为依托咪酯药物滥用类案件的鉴定提供可靠的检测手段和实验数据。
1 材料与方法
1.1 主要仪器与试剂
Triple Quad™ 5500+三重四极杆液质联用系统—QTRAP™ Ready(美国AB Sciex公司),Multi Reax混匀器(德国Heidolph公司),BRANSON 1210超声波清洗机(美国Emerson公司),3-18K型高速冷冻离心机(德国Sigma公司)。
甲醇、乙腈(均为HPLC级,美国Thermo Fisher Scientific公司),实验用超纯水由Milli-Q® IQ 7003智能环保超纯水系统(德国Merck KGaA公司)制备,依托咪酯和依托咪酯酸标准品溶液质量浓度均为1.0 mg/mL(广州谱登生物科技有限公司)。
1.2 标准储备液的配制
精确量取适量依托咪酯和依托咪酯酸标准品溶液,用甲醇稀释至0.1 mg/mL,密封,置于-20 ℃保存。实验中根据检测需求用甲醇对标准品溶液进行稀释,配制成系列浓度标准工作溶液。
1.3 样品前处理
取0.2 mL尿液于离心管中,加入0.8 mL乙腈,涡旋振荡5 min,超声处理5 min,以离心半径99 mm,10 000 r/min高速离心10 min,取上清液过0.22 μm滤膜,待分析。若实际尿液样品中目标物浓度过高,可用相同的空白基质稀释样品后进行检测。
1.4 仪器条件
色谱条件:使用ZORBAX SB-C18色谱柱(100 mm×2.1 mm,1.8 μm;美国Agilent公司),柱温40 ℃,进样量2 μL,流速0.4 mL/min;流动相A为0.1%甲酸水溶液,流动相B为乙腈,梯度洗脱程序见表1。
表1 梯度洗脱程序 (%)
Tab. 1
| 时间/min | 流动相A | 流动相B |
|---|---|---|
| 0.01 | 95 | 5 |
| 1 | 95 | 5 |
| 8 | 5 | 95 |
| 9 | 5 | 95 |
| 9.01 | 95 | 5 |
质谱条件:采用电喷雾电离(electrospray ionization,ESI)正离子模式扫描,多反应监测(multiple reaction monitoring,MRM)模式检测;电喷雾电压5 500 V;离子源温度500 ℃;气帘气(CUR) 40 psi,喷雾气(GS1) 55 psi,辅助加热气(GS2) 55 psi,均为高纯氮气。
1.5 方法学验证
选择性:取10份不同来源的空白尿液样品,观察尿液中添加5 ng/mL依托咪酯和10 ng/mL依托咪酯酸的出峰情况,以确认目标物的保留时间是否存在干扰。
线性、LOD和LOQ:添加依托咪酯和依托咪酯酸标准工作溶液至空白尿液中,制成系列质量浓度添加样品,最终质量浓度分别达到0.5、1、2、5、10、20、50 ng/mL(依托咪酯)和1、2、5、10、20、50、100 ng/mL(依托咪酯酸)。按照1.3节方法处理后,在1.4节条件下,分别以添加的依托咪酯和依托咪酯酸质量浓度为横坐标(x)、峰面积为纵坐标(y)绘制标准曲线,建立线性回归方程[选用权重系数(w)补偿异方差性,w=1/x2]。每个浓度点的添加样品独立重复5次,空白样品在最高浓度点后进样以评价残留效应。以信噪比(S/N)≥3时的样品最低质量浓度为LOD,以S/N≥10时的样品质量浓度为LOQ。
基质效应及提取回收率的计算公式如下:
式中,A为空白尿液按照1.3节方法处理后添加低(0.5 ng/mL)、中(5 ng/mL)、高(50 ng/mL) 3个质量浓度的依托咪酯溶液或低(1 ng/mL)、中(10 ng/mL)、高(100 ng/mL) 3个质量浓度的依托咪酯酸溶液所测得的峰面积;B为空白尿液先添加该3个质量浓度的依托咪酯或依托咪酯酸溶液,再按照1.3节方法处理后测得的峰面积;C为相应质量浓度的依托咪酯或依托咪酯酸标准品溶液所测得的峰面积。每个质量浓度点使用6个不同来源的空白尿液样品并重复进样 6次。若基质效应超出±25%,则应增加不同来源的空白样品考察基质效应是否对LOD、LOQ、准确度及精密度产生影响[15-16]。
精密度为样品测定值的标准偏差与平均值的比值,准确度为测定的平均值与参考值的百分比。选取低(0.5 ng/mL)、中(5 ng/mL)、高(50 ng/mL) 3个质量浓度的依托咪酯溶液和低(1 ng/mL)、中(10 ng/mL)、高(100 ng/mL) 3个质量浓度的依托咪酯酸溶液制备质控样品,每天选取各质量浓度的样品配制6个质控样品分别进行测定,并连续平行操作3 d。日内准确度和日间准确度分别由1 d内测定的平均值和3 d内测定的平均值与相应参考值的百分比计算得出。日内精密度和日间精密度分别是1 d内和3 d内实验测定值的标准偏差与相应平均值的比值。准确度及精密度的检测结果应分别控制在85%~115%和±15%之内,LOQ水平时则在80%~120%和±20%之内[15-16]。
稳定性主要考察冻融稳定性和长期稳定性。其中冻融稳定性考察低(0.5 ng/mL)、中(5 ng/mL)、高(50 ng/mL) 3个质量浓度的依托咪酯溶液(n=9)和低(1 ng/mL)、中(10 ng/mL)、高(100 ng/mL) 3个质量浓度的依托咪酯酸溶液(n=9),在-20 ℃下冷冻24 h,然后室温放置24 h融化,重复3个冻融循环后进行测定;长期稳定性考察低(0.5 ng/mL)、中(5 ng/mL)、高(50 ng/mL) 3个质量浓度的依托咪酯溶液(n=3)和低(1 ng/mL)、中(10 ng/mL)、高(100 ng/mL) 3个质量浓度的依托咪酯酸溶液(n=3),在-20 ℃下保存7 d、14 d及28 d后进行测定。
配制空白尿液添加样品(依托咪酯50 μg/mL和依托咪酯酸100 μg/mL)考察稀释可靠性。用空白尿液基质稀释该样品1 000倍,按照方法学验证中准确度和精密度的分析方法分析3个批次。
2 结果与讨论
2.1 质谱条件优化
表2 优化后的依托咪酯和依托咪酯酸HPLC-MS/MS分析参数
Tab. 2
| 目标物 | 保留时间/min | 母离子(m/z) | 子离子(m/z) | 去簇电压/V | 碰撞能量/eV |
|---|---|---|---|---|---|
| 依托咪酯 | 5.27 | 245.0 | 141.01) | 40.0 | 15.5 |
| 105.0 | 40.0 | 35.0 | |||
| 依托咪酯酸 | 3.19 | 217.1 | 95.01) | 28.0 | 32.0 |
| 105.0 | 28.0 | 33.0 |
图3
图3
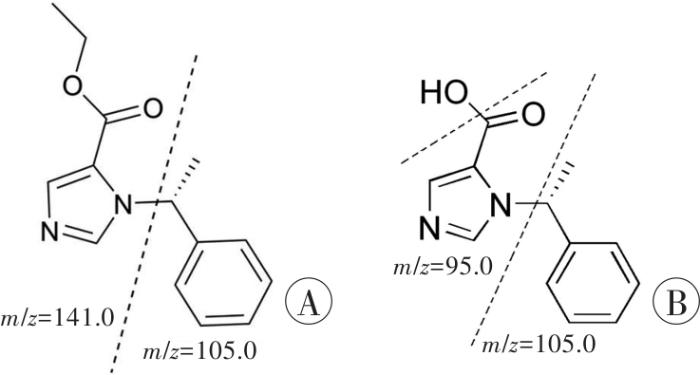
目标化合物在MRM模式下的碎片化结果
A:依托咪酯;B:依托咪酯酸。虚线表示目标物离子化碎片的断键方式。
Fig. 3
Fragmentation of target substances under MRM mode
2.2 方法学验证结果
2.2.1 选择性
图4
图4
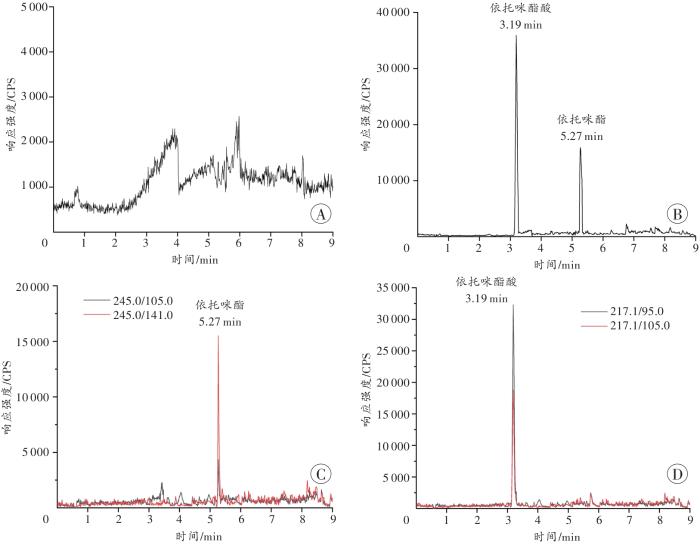
尿液样品的TIC和MRM色谱图
A:空白尿液的TIC图;B:空白尿液中添加5 ng/mL依托咪酯和10 ng/mL依托咪酯酸标准混合溶液的TIC图;C:空白尿液中添加5 ng/mL依托咪酯的MRM图;D:空白尿液中添加10 ng/mL依托咪酯酸的尿液MRM图。
Fig. 4
TIC and MRM chromatograms of urine samples
2.2.2 线性范围、LOD和LOQ
依托咪酯和依托咪酯酸的线性范围、LOD和LOQ见表3。其中,依托咪酯的LOD为0.2 ng/mL、LOQ为0.5 ng/mL,依托咪酯酸的LOD为0.5 ng/mL、LOQ为1 ng/mL。
表3 尿液中添加依托咪酯和依托咪酯酸的线性范围、LOD和LOQ
Tab. 3
| 目标物 | 线性方程 | 线性范围/(ng·mL-1) | 相关系数(r) | LOD/(ng·mL-1) | LOQ/(ng·mL-1) |
|---|---|---|---|---|---|
| 依托咪酯 | y=8 144.8 x-2 669.4 | 0.5~50 | 0.995 0 | 0.2 | 0.5 |
| 依托咪酯酸 | y=7 779 x+29 864 | 1~100 | 0.998 8 | 0.5 | 1 |
以尿液中添加依托咪酯的质量浓度为横坐标、峰面积为纵坐标构建标准曲线,在0.5~50 ng/mL质量浓度范围内线性关系良好(r=0.995 0);以尿液中添加依托咪酯酸的质量浓度为横坐标、峰面积为纵坐标构建标准曲线,在1~100 ng/mL质量浓度范围内线性关系良好(r=0.998 8);且依托咪酯在0.5~50 ng/mL和依托咪酯酸在1~100 ng/mL质量浓度范围内均未见残留效应。本研究所建方法的线性范围可满足法医毒物分析方法验证通则的需求,即线性方程的相关系数不小于0.99[15]。
2.2.3 基质效应、回收率、稳定性及稀释可靠性
依托咪酯和依托咪酯酸在尿液样品中的基质效应、回收率和稳定性见表4。
表4 尿液中添加依托咪酯和依托咪酯酸的基质效应、回收率及稳定性 (%)
Tab. 4
| 目标物 | 质量浓度/(ng·mL-1) | 基质效应 | 回收率 | 冻融稳定性 | 长期稳定性 | ||
|---|---|---|---|---|---|---|---|
| 7 d | 14 d | 28 d | |||||
| 依托咪酯 | 0.5 | 18.47 | 96.64 | 110.23 | 103.51 | 110.65 | 91.26 |
| 5 | 7.29 | 93.07 | 102.34 | 100.26 | 97.12 | 89.84 | |
| 50 | 5.42 | 84.25 | 98.49 | 99.55 | 97.24 | 90.75 | |
| 依托咪酯酸 | 1 | 8.29 | 107.43 | 91.77 | 101.91 | 90.68 | 105.79 |
| 10 | 7.11 | 110.26 | 102.31 | 96.36 | 93.80 | 92.16 | |
| 100 | 10.73 | 97.82 | 103.68 | 100.43 | 94.01 | 88.23 | |
在低、中、高3个质量浓度下,尿液中依托咪酯的提取回收率分别为96.64%、93.07%和84.25%,依托咪酯酸的提取回收率分别为107.43%、110.26%和97.82%,表明本研究的前处理方法对目标物的提取损失较小,并随着样品质量浓度的增加,提取回收率有轻微的降低。
依托咪酯的冻融稳定性和长期稳定性分别在98.49%~110.23%和89.84%~110.65%范围内,依托咪酯酸的冻融稳定性和长期稳定性分别在91.77%~103.68%和88.23%~105.79%范围内。
2.2.4 准确度和精密度
表5 尿液中添加依托咪酯和依托咪酯酸的准确度和精密度 (%)
Tab. 5
| 目标物 | 质量浓度/(ng·mL-1) | 准确度 | 精密度 | ||
|---|---|---|---|---|---|
| 日内(n=6) | 日间(n=18) | 日内(n=6) | 日间(n=18) | ||
| 依托咪酯 | 0.5 | 110.80 | 109.53 | 9.35 | 1.61 |
| 5 | 91.44 | 95.18 | 6.54 | 5.80 | |
| 50 | 100.14 | 100.96 | 5.13 | 1.16 | |
| 依托咪酯酸 | 1 | 95.66 | 90.42 | 3.49 | 10.08 |
| 10 | 98.72 | 107.24 | 3.28 | 9.77 | |
| 100 | 100.22 | 99.30 | 0.56 | 4.88 | |
2.3 案例应用
按本研究方法对某地区一吸食过量依托咪酯死者的尿液样本进行处理及检测,成功检出依托咪酯和依托咪酯酸成分,经计算,该死者尿液中依托咪酯质量浓度为8.82 μg/mL,依托咪酯酸质量浓度为27.88 μg/mL。据报道[18],全血中依托咪酯的治疗质量浓度范围为0.35~0.66 μg/mL,作为静脉麻醉剂使用后在尿液中的质量浓度为6~11 ng/mL。上述结果为该死者生前服用过依托咪酯提供了客观证据。
2.4 小结
本研究采用乙腈沉淀蛋白的方式对尿液样品进行前处理,建立了尿液中依托咪酯和依托咪酯酸的HPLC-MS/MS分析方法。该方法前处理简单、灵敏度高、线性范围宽,且选择性、准确度、精密度、稳定性等指标均满足生物样品定性定量分析要求,可应用于法庭科学领域尿液中依托咪酯和依托咪酯酸的检测。
参考文献
Dl-1-(1-arylalkyl)imidazole-5-carboxylate esters. A novel type of hypnotic agents
[J].
Structure-activity relationship of etomidate derivatives at the GABA(A) receptor: Comparison with binding to 11beta-hydroxylase
[J].
Sympathetic responses to induction of anesthesia in humans with propofol or etomidate
[J].
Suicide committed by a paramedic using a cocktail of drugs: Morphine, etomidate, diazepam and rocuronium. Case report and review of literature
[J].
The pharmacology of cyclopropyl-methoxycarbonyl metomidate: A comparison with propofol
[J].
An etomidate analogue with less adrenocortical suppression, stable hemodynamics, and improved behavioral recovery in rats
[J].
Determination of etomidate and etomidate acid in hair using liquid chromatography-tandem mass spectrometry
[J].
依托咪酯药理作用、药物代谢动力学及毒理学研究
[J].
Study of pharmacological action, pharmacokinetics and toxicology of etomidate
[J].
High-performance liquid chromatographic determination of etomidate in plasma
[J].
Determination of etomidate in human plasma by high-performance liquid chromatography
[J].
Simultaneous determination of etomidate and its major metabolite, etomidate acid, in urine using dilute and shoot liquid chromatography-tandem mass spectrometry
[J].
Gas chromatographic-mass spectrometric determination of etomidate in mouse brain
[J].
LC-MS/MS法测定血液中卡马西平及其代谢物
[J].
Detection of carbamazepine and its metabolites in blood samples by LC-MS/MS
[J].
A simple and efficient high-performance liquid chromatographic assay for etomidate in plasma
[J].
生物样品分析方法的有效性验证
[J].
How to validate a bio-analytical method
[J].
HPLC-MS/MS法快速测定电子烟油中58种合成大麻素
[J].
58 synthetic cannabinoids rapidly determined from electronic cigarette oil by HPLC-MS/MS
[J].
Determination of etomidate in human postmortem fluids and tissues
[R/OL]. (