药物辅助犯罪(drug-facilitated crime,DFC)是一个总称,包括受精神药物影响实施的强奸或其他形式的性侵犯、抢劫、勒索钱财以及故意虐待老人或儿童的犯罪行为[1]。药物辅助性犯罪(drug-facilitated sexual assault,DFSA)是药物辅助犯罪案件的一个子集,在DFSA案件中,具有精神活性的药物被用来改变一个人的意识和行为,从而实施性犯罪,涉及的物质主要包括乙醇、γ-羟基丁酸、苯二氮䓬类药物、非苯二氮䓬类新型镇静安眠药物(Z-药物)等[2-4]。然而,DFSA案件给法医毒物学者带来了挑战,因为从案发到检测通常经历时间较长,且这类案件药物剂量较低,随着体内代谢的消除,药物在血液和尿液中无法检出[5]。为了延长检测窗口,毛发分析已成为法医毒物学和临床毒理学领域解决DFSA案件必不可少的技术手段[6-7]。
在既往研究[12]中,本课题组应用两个DFSA案例比较了毛发微分段分析与常规的1 cm分段分析方法,结果表明,微分段分析可以提高毛发中药物检测的实用性,增强DFSA案件的证据力。近年来,基质辅助激光解吸电离-质谱成像(matrix-assisted laser desorption ionization-mass spectrometry imaging,MALDI-MSI)技术由于其高分辨率、可原位分析、结果可视化等优势,在单根头发的药物分布研究中受到广泛关注[13-15]。然而,液相色谱-串联质谱(liquid chromatography-tandem mass spectrometry,LC-MS/MS)对生物样品中药物定性和定量分析的灵敏度要优于MALDI-MSI[16]。因此,采用LC-MS/MS法能够实现对于亚毫米头发片段中的药物检测和分析。本研究旨在建立一种覆盖42种常见精神活性物质的单根头发微分段分析方法并应用于单次服用唑吡坦的志愿者头发样本,以探究单根头发微分段分析方法在解决DFSA案件中的可行性。
1 材料与方法
1.1 主要仪器与试剂
QTRAP 6500+三重四极杆线性离子阱复合质谱系统(美国AB Sciex公司)配备AcquityTM Ultra performance LC I-CLASS超高效液相色谱仪(美国Waters公司),SB-2200-T超声波清洗仪(深圳市洁盟清洗设备有限公司)。
42种精神活性物质及3种内标的标准溶液均为质量浓度为1 mg/mL的甲醇溶液。苯海拉明、地芬尼多、东莨菪碱、安替比林购于上海安谱实验科技股份有限公司,苯丙胺、甲基苯丙胺、氯胺酮、吗啡、O6-单乙酰吗啡、可卡因、苯甲酰爱康宁、麦角二乙胺、芬太尼、氟硝西泮、7-氨基氟硝西泮、三唑仑、α-羟基三唑仑、可待因、地西泮、去甲地西泮、替马西泮、奥沙西泮、阿普唑仑、α-羟基阿普唑仑、氯硝西泮、7-氨基氯硝西泮、艾司唑仑、劳拉西泮、咪达唑仑、硝西泮、7-氨基硝西泮、唑吡坦、西酞普兰、右美沙芬、氯氮平、右美托咪定、曲马多、卡马西平、奥卡西平、尼美西泮、喹硫平、米氮平以及3种内标(氯胺酮-d4,地西泮-d5,喹硫平-d8)的对照品购自美国Cerilliant公司,思诺思酒石酸唑吡坦片(10 mg,含10 mg酒石酸唑吡坦/片)购自赛诺菲(杭州)制药有限公司。二硫苏糖醇(dithiothreitol,DTT)、甲醇(色谱纯)和乙腈(色谱纯)购自美国Sigma-Aldrich公司,98%甲酸溶液和98%乙酸铵溶液购自瑞士Fluka公司,超纯水由Milli-Q Advantage A10超纯水系统(美国Millipore公司)制备。
1.2 溶液配制
1.2.1 混合标准物质工作液配制
取42种精神活性物质的标准物质适量,加入甲醇配制成质量浓度为1 μg/mL的混合标准物质工作液。随后用甲醇稀释成质量浓度为16~40 000 pg/mL的混合工作溶液。
1.2.2 混合内标工作液配制
取3种内标对照品适量,加入甲醇配制成质量浓度为10 μg/mL的混合内标工作液。随后用甲醇稀释成质量浓度为0.5 ng/mL的混合内标工作溶液。
所有工作溶液在使用前均置于-20 ℃冰箱中保存。
1.2.3 提取溶液配制
毛发提取介质为V甲醇∶V乙腈∶V2 mmol/L甲酸铵(8%乙腈,pH=5.3)=25∶25∶50的混合物。提取溶剂为将DTT溶解于毛发提取介质(extraction medium,EM)溶液中制备成的质量浓度为10 mg/mL的DTT-EM溶液。
1.3 样本来源
空白头发样本采集自10名未摄入上述精神活性物质的健康志愿者,用于制备校正曲线及质量控制样品。
志愿者头发样本(黑色,8 cm)来自一名本实验室工作人员(女性,32岁),在本研究之前未服用过精神药品,在本研究中单次服用唑吡坦后28 d,用镊子从后枕部拔取5根头发,标记根部,4 ℃保存供分析。
本研究已通过司法鉴定科学研究院伦理委员会审批,实验前告知志愿者药物实验风险并签署知情同意书。
1.4 样本前处理
用去离子水和丙酮擦拭头发样本,以避免外部污染干扰分析,室温下干燥。然后将单根头发粘在胶带上,用外科手术剪刀在30倍的放大镜下将其剪成长0.4 mm的片段,该长度与头发每日的生长长度[17]大致一致。将每个0.4 mm的头发片段置于200 µL的微量离心管中,加入5 μL内标和20 μL DTT-EM溶液,超声1 h,浸泡20 h。取上清液供LC-MS/MS分析。对于实验头发样本,将5根头发的近根端2 cm分成50段0.4 mm的片段,标记为S1、S2……S50,并按照上述方法进行提取。
1.5 仪器条件
1.5.1 色谱条件
色谱柱为Allure PFPP柱(100 mm×2.1 mm,5 μm;美国Restek公司)。流动相A为20 mmol/L乙酸铵、0.1%甲酸和5%乙腈的水溶液,流动相B为乙腈。采用线性梯度洗脱,洗脱程序见表1。自动进样器温度为4 ℃,进样量为10 μL。
表1 梯度洗脱程序
Tab. 1
| 时间/min | 流速/(mL·min-1) | 流动相A/% | 流动相B/% |
|---|---|---|---|
| 0 | 0.2 | 75 | 25 |
| 1.0 | 0.2 | 75 | 25 |
| 8.0 | 0.4 | 50 | 50 |
| 14.0 | 0.4 | 10 | 90 |
| 14.5 | 0.4 | 75 | 25 |
| 16.0 | 0.2 | 75 | 25 |
1.5.2 质谱条件
采用电喷雾离子源正离子(positive electrospray ionization,ESI+)模式,在多反应监测(multiple reaction monitoring,MRM)模式下采集数据。ESI参数设置如下:离子源温度450 ℃;气帘气(N2) 30 psi;离子喷射电压5 500 V,碰撞室出口电压10 V、入口电压10 V;离子源气体1(GS1) 35 psi,离子源气体2(GS2) 35 psi。MRM参数和保留时间见表2。
表2 42种精神活性物质及3种内标的MRM参数和保留时间
Tab. 2
| 化合物 | 前体离子(m/z) | 产物离子(m/z) | 去簇电压/V | 碰撞能量/eV | 保留时间/min |
|---|---|---|---|---|---|
| 苯丙胺 | 136.1 | 119.11)/91.1 | 60 | 11/22 | 5.24 |
| 甲基苯丙胺 | 150.1 | 119.11)/91.1 | 50 | 14/23 | 6.39 |
| 氯胺酮 | 238.1 | 179.11)/125.1 | 60 | 24/35 | 6.63 |
| 吗啡 | 286.1 | 201.21)/165.3 | 80 | 35/52 | 2.62 |
| O6-单乙酰吗啡 | 328.1 | 211.31)/165.3 | 80 | 36/48 | 4.70 |
| 可卡因 | 304.1 | 182.21)/150.2 | 60 | 28/35 | 6.56 |
| 苯甲酰爱康宁 | 290.2 | 168.31)/105.2 | 70 | 26/43 | 1.40 |
| 麦角二乙胺 | 324.2 | 223.21)/208.2 | 60 | 33/43 | 5.77 |
| 芬太尼 | 337.2 | 188.31)/104.9 | 20 | 27/13 | 3.76 |
| 地芬尼多 | 310.0 | 292.61)/129.4 | 60 | 26/40 | 8.03 |
| 氟硝西泮 | 314.2 | 268.31)/239.3 | 60 | 35/45 | 6.15 |
| 7-氨基氟硝西泮 | 284.2 | 135.21)/226.2 | 60 | 39/41 | 3.62 |
| 三唑仑 | 343.2 | 308.21)/315.2 | 60 | 36/35 | 5.46 |
| α-羟基三唑仑 | 359.2 | 331.21)/176.1 | 60 | 38/37 | 4.13 |
| 可待因 | 300.2 | 199.21)/165.3 | 80 | 40/52 | 3.78 |
| 地西泮 | 285.1 | 193.31)/154.1 | 80 | 45/36 | 6.65 |
| 去甲地西泮 | 271.2 | 140.21)/208.1 | 70 | 36/36 | 5.44 |
| 替马西泮 | 301.2 | 255.21)/283.1 | 70 | 36/19 | 5.52 |
| 奥沙西泮 | 287.2 | 241.21)/269.3 | 50 | 31/21 | 4.42 |
| 阿普唑仑 | 309.1 | 281.11)/274.2 | 60 | 33/32 | 5.46 |
| α-羟基阿普唑仑 | 325.2 | 297.21)/279.2 | 70 | 35/33 | 4.17 |
| 氯硝西泮 | 316.2 | 270.11)/214.1 | 60 | 36/49 | 5.36 |
| 7-氨基氯硝西泮 | 286.1 | 222.21)/250.1 | 40 | 34/25 | 2.92 |
| 艾司唑仑 | 295.2 | 267.31)/205.2 | 50 | 34/53 | 4.84 |
| 劳拉西泮 | 321.1 | 275.11)/303.1 | 50 | 30/21 | 4.60 |
| 咪达唑仑 | 326.2 | 291.41)/244.2 | 50 | 37/37 | 9.39 |
| 硝西泮 | 282.2 | 236.21)/180.2 | 50 | 35/32 | 5.05 |
| 7-氨基硝西泮 | 252.1 | 121.11)/146.2 | 60 | 52/37 | 2.90 |
| 唑吡坦 | 308.1 | 235.11)/263.2 | 40 | 38/53 | 9.29 |
| 西酞普兰 | 325.3 | 109.21)/262.0 | 60 | 35/41 | 13.32 |
| 苯海拉明 | 256.2 | 167.21)/165.2 | 30 | 26/17 | 13.64 |
| 右美沙芬 | 272.3 | 147.21)/213.3 | 60 | 54/42 | 12.31 |
| 氯氮平 | 327.3 | 270.11)/296.3 | 70 | 28/32 | 10.90 |
| 东莨菪碱 | 304.3 | 138.31)/156.3 | 60 | 33/31 | 4.34 |
| 右美托咪定 | 201.1 | 68.11)/94.8 | 60 | 23/40 | 9.39 |
| 曲马多 | 264.2 | 58.01)/246.2 | 50 | 24/37 | 8.46 |
| 安替比林 | 189.0 | 56.01)/77.0 | 60 | 16/27 | 2.59 |
| 卡马西平 | 237.3 | 194.31)/192.3 | 60 | 37/26 | 4.16 |
| 奥卡西平 | 253.0 | 235.91)/208.1 | 70 | 32/19 | 3.47 |
| 尼美西泮 | 296.1 | 250.21)/222.1 | 70 | 20/36 | 6.13 |
| 喹硫平 | 384.4 | 253.11)/221.0 | 54 | 30/35 | 10.10 |
| 米氮平 | 266.1 | 195.11)/208.8 | 80 | 37/35 | 7.81 |
| 氯胺酮-d4 | 242.2 | 183.11)/129.2 | 60 | 26/40 | 6.81 |
| 地西泮-d5 | 290.2 | 198.21)/154.4 | 60 | 46/40 | 6.50 |
| 喹硫平-d8 | 392.2 | 258.11)/226.1 | 40 | 31/50 | 10.30 |
1.6 方法学验证
1.6.1 选择性
取10份不同来源的空白头发样品,分别按照1.4节方法进行样品前处理,考察头发样品中的内源性物质是否干扰42种精神活性物质的测定。
1.6.2 线性、检出限和定量限
校准曲线范围从每个化合物的最低定量限到500 pg/mm。将工作溶液添加到空白的单根0.4 mm头发片段中,配制成浓度为0.5、1、2、5、10、20、50、100、250和500 pg/mm的加标头发样品,并对每个校准水平进行3次重复评估。以每个分析物的浓度为横坐标(x),以定量离子对与内标的峰面积比为纵坐标(y),使用加权最小二乘法(1/x)进行回归计算获得曲线方程,相关系数(r)至少为0.99。以信噪比(S/N)≥3为检出限(limit of detection,LOD),以S/N≥10且精密度的变异系数小于20%,准确度在80%和120%之间为最低定量限(lower limit of quantitation,LLOQ)[18]。
1.6.3 精密度和准确度
在0.4 mm空白头发样品中加入42种精神活性物质的混合工作溶液,配制成浓度为LLOQ和250 pg/mm两个浓度的质量控制(quality control,QC)样品,每个浓度点制备6个平行样品,按照1.4节方法进行样本前处理,连续测定4 d。精密度用相对标准偏差(relative standard deviation,RSD)来评估。经线性方程计算的测定值与实际添加混合工作溶液的浓度的百分比为准确度。要求LLOQ样品的精密度不超过20%,其余QC样品的精密度不超过15%;LLOQ样品的准确度在80%~120%,其余QC样品的准确度在85%~115%[18]。
1.6.4 基质效应和提取回收率
按照MATUSZEWSKI等[19]提出的方法考察基质效应和提取回收率。选取低浓度(LLOQ)和高浓度(250 pg/mm)作为QC浓度进行考察。将超声和浸泡处理前的加标头发样品中各化合物的峰面积记为SA,超声和浸泡处理后的加标头发样品中各化合物的峰面积记为SB,在相应浓度的纯标准溶液中各化合物的绝对峰面积记为SC。用生成峰面积SB/SC×100%计算基质效应,用生成峰面积SA/SB×100%计算提取回收率。
2 结果与讨论
2.1 微分段分析浓度单位的选择
关于单根头发微分段分析单位的选择,既往研究[20-21]中报道不一。由于0.4 mm的头发片段质量较小,实验室常规的称量设备无法直接对其质量进行精确称量。KUWAYAMA等[20]提出可以测量1根头发的长度并称量其质量,根据其质量从而估计每一段头发的平均质量。该研究对22根头发进行了称重并测量,0.4 mm头发片段的质量在2.29~6.42 μg。然而,WIEDFELD等[21]认为,即使根据头发片段的平均质量进行计算,个体间和个体内头发直径的差异也会影响浓度的准确性。此外,清洗、烫染和天气变化可能会增加头发角质层的损伤和降解,不同发丝间的含水量也可能不同,质量可能存在2~3倍的差异。因此,以长度为单位对浓度的反映更为准确且方便。
2.2 方法学验证
2.2.1 选择性
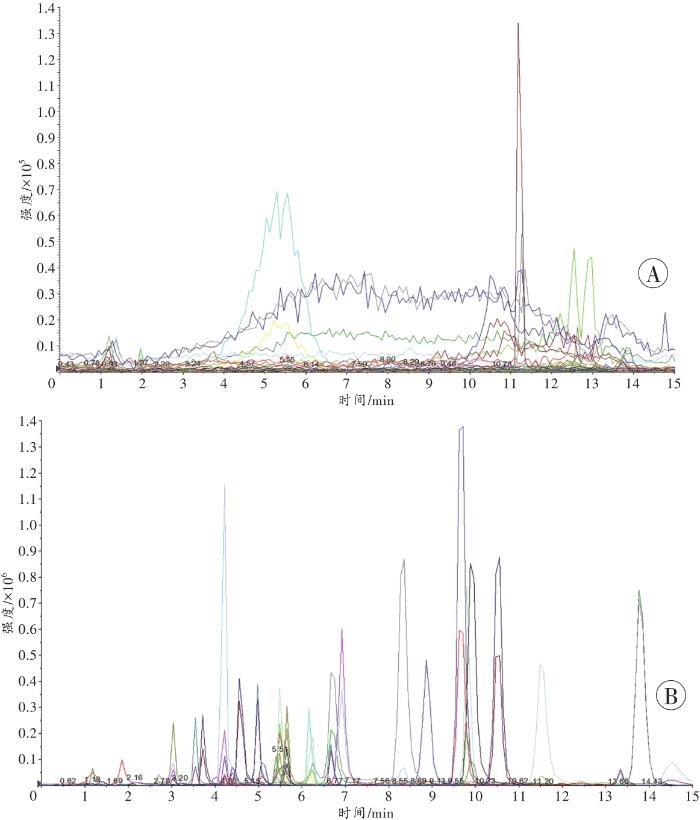
10份不同来源的空白头发样品经样品前处理后,在待测化合物对应的保留时间处均无内源性干扰以及内标的干扰,说明该方法的选择性良好。空白头发与空白头发添加20 pg/mm 42种精神活性物质的色谱图见图1。
图1
图1
空白头发(A)与空白头发添加20 pg/mm 42种精神活性物质(B)的色谱图
Fig. 1
The chromatograms of hair collecting before administration (A) and 42 psychoactive substances spiked at 20 pg/mm (B)
2.2.2 线性、LOD和LLOQ
本研究中所有化合物在各自线性范围内线性关系良好(r>0.99)。LOD为0.2~10 pg/mm,LLOQ为0.5~20 pg/mm。在该方法覆盖的42种化合物中,26种物质(61.9%)的LLOQ≤5 pg/mm,8种物质(19.0%)的LLOQ≤1 pg/mm。各化合物的回归方程、相关系数(r)、LOD和LLOQ见表3。
表3 头发中42种精神活性物质的回归方程、相关系数(r)、LOD和LLOQ
Tab. 3
| 化合物 | 线性范围/ (pg·mm-1) | 回归方程 | 相关系数(r) | LOD/ (pg·mm-1) | LLOQ/ (pg·mm-1) | 内标 |
|---|---|---|---|---|---|---|
| 苯丙胺 | 5~500 | y=0.207 83 x+3.045 54 | 0.993 96 | 2 | 5 | 氯胺酮-d4 |
| 甲基苯丙胺 | 20~500 | y=0.744 31 x+4.803 91 | 0.994 28 | 5 | 20 | 氯胺酮-d4 |
| 氯胺酮 | 10~500 | y=1.216 12 x+2.136 96 | 0.997 66 | 2 | 10 | 氯胺酮-d4 |
| 吗啡 | 20~500 | y=0.021 54 x+0.660 82 | 0.993 31 | 10 | 20 | 氯胺酮-d4 |
| 甲基苯丙胺 | 20~500 | y=0.744 31 x+4.803 91 | 0.994 28 | 5 | 20 | 氯胺酮-d4 |
| 氯胺酮 | 10~500 | y=1.216 12 x+2.136 96 | 0.997 66 | 2 | 10 | 氯胺酮-d4 |
| O6-单乙酰吗啡 | 20~500 | y=0.004 43 x+0.546 90 | 0.993 02 | 5 | 20 | 氯胺酮-d4 |
| 可卡因 | 5~500 | y=1.951 38 x+3.168 50 | 0.994 17 | 2 | 5 | 氯胺酮-d4 |
| 苯甲酰爱康宁 | 2~500 | y=2.720 58 x+0.919 45 | 0.997 93 | 1 | 2 | 氯胺酮-d4 |
| 麦角二乙胺 | 1~500 | y=2.354 68 x+0.426 31 | 0.997 55 | 0.5 | 1 | 氯胺酮-d4 |
| 芬太尼 | 20~500 | y=1.152 65 x-9.790 53 | 0.990 28 | 10 | 20 | 氯胺酮-d4 |
| 地芬尼多 | 10~500 | y=1.332 11 x+2.886 06 | 0.993 25 | 2 | 10 | 喹硫平-d8 |
| 氟硝西泮 | 2~500 | y=0.042 87 x-0.063 26 | 0.995 18 | 0.5 | 2 | 地西泮-d5 |
| 7-氨基氟硝西泮 | 2~500 | y=0.072 76 x-0.146 79 | 0.996 68 | 0.5 | 2 | 地西泮-d5 |
| 三唑仑 | 1~500 | y=0.055 27 x-0.031 23 | 0.994 24 | 0.2 | 1 | 地西泮-d5 |
| α-羟基三唑仑 | 5~500 | y=0.008 25 x+0.003 83 | 0.994 26 | 1 | 5 | 地西泮-d5 |
| 可待因 | 20~500 | y=0.057 99 x+1.219 88 | 0.998 88 | 5 | 20 | 地西泮-d5 |
| 地西泮 | 1~500 | y=0.310 37 x+1.076 27 | 0.995 08 | 0.2 | 1 | 地西泮-d5 |
| 去甲地西泮 | 5~500 | y=0.117 61 x+2.319 53 | 0.994 32 | 1 | 5 | 地西泮-d5 |
| 替马西泮 | 10~500 | y=0.543 24 x+1.570 80 | 0.995 76 | 5 | 10 | 地西泮-d5 |
| 奥沙西泮 | 20~500 | y=0.077 60 x+6.031 51 | 0.997 49 | 10 | 20 | 地西泮-d5 |
| 阿普唑仑 | 2~500 | y=0.505 37 x+1.623 54 | 0.995 75 | 0.5 | 2 | 地西泮-d5 |
| α-羟基阿普唑仑 | 10~500 | y=0.128 46 x+0.991 37 | 0.991 39 | 2 | 10 | 地西泮-d5 |
| 氯硝西泮 | 5~500 | y=0.196 84 x+1.842 02 | 0.995 11 | 1 | 5 | 地西泮-d5 |
| 7-氨基氯硝西泮 | 2~500 | y=0.160 57 x+1.340 30 | 0.993 32 | 1 | 2 | 地西泮-d5 |
| 艾司唑仑 | 1~500 | y=1.336 01 x+0.224 92 | 0.998 56 | 0.2 | 1 | 地西泮-d5 |
| 劳拉西泮 | 20~500 | y=0.049 56 x+0.462 25 | 0.996 62 | 10 | 20 | 地西泮-d5 |
| 咪达唑仑 | 1~500 | y=2.790 51 x+0.312 17 | 0.997 59 | 0.5 | 1 | 地西泮-d5 |
| 硝西泮 | 5~500 | y=0.234 00 x+1.193 09 | 0.994 09 | 2 | 5 | 地西泮-d5 |
| 7-氨基硝西泮 | 10~500 | y=0.542 20 x+8.245 20 | 0.993 77 | 5 | 10 | 地西泮-d5 |
| 唑吡坦 | 0.5~500 | y=6.173 96 x+0.222 13 | 0.995 16 | 0.1 | 0.5 | 地西泮-d5 |
| 西酞普兰 | 2~500 | y=7.322 17 x+1.558 15 | 0.998 04 | 0.5 | 2 | 喹硫平-d8 |
| 苯海拉明 | 2~500 | y=0.785 10 x+1.299 34 | 0.997 54 | 1 | 2 | 喹硫平-d8 |
| 右美沙芬 | 10~500 | y=0.243 66 x+7.096 43 | 0.993 61 | 2 | 10 | 喹硫平-d8 |
| 氯氮平 | 2~500 | y=2.494 10 x+6.650 52 | 0.993 80 | 1 | 2 | 喹硫平-d8 |
| 东莨菪碱 | 0.5~500 | y=1.567 98 x-0.120 40 | 0.996 04 | 0.2 | 0.5 | 喹硫平-d8 |
| 右美托咪定 | 5~500 | y=0.333 05 x+2.030 27 | 0.994 15 | 2 | 5 | 喹硫平-d8 |
| 曲马多 | 20~500 | y=0.557 97 x+7.067 36 | 0.996 66 | 10 | 20 | 喹硫平-d8 |
| 安替比林 | 20~500 | y=0.019 51 x+2.472 81 | 0.994 99 | 5 | 20 | 喹硫平-d8 |
| 卡马西平 | 5~500 | y=2.121 50 x+1.417 83 | 0.997 63 | 2 | 5 | 喹硫平-d8 |
| 奥卡西平 | 10~500 | y=0.335 85 x+6.422 52 | 0.994 89 | 5 | 10 | 喹硫平-d8 |
| 尼美西泮 | 2~500 | y=0.519 45 x+0.488 19 | 0.995 54 | 1 | 2 | 地西泮-d5 |
| 喹硫平 | 2~500 | y=6.655 51 x+1.312 71 | 0.994 33 | 1 | 2 | 喹硫平-d8 |
| 米氮平 | 0.5~500 | y=4.556 82 x+0.015 92 | 0.996 80 | 0.2 | 0.5 | 喹硫平-d8 |
2.2.3 精密度和准确度
本研究中各化合物的精密度和准确度见表4。该方法的日内精密度为1.5%~11.8%,日内准确度为86.5%~105.7%,日间精密度为2.8%~12.7%,日间准确度为88.2%~109.2%。精密度均在15%以内,准确度均在85%~115%,表明该方法的精密度和准确度良好。
表4 头发中42种精神活性物质的精密度、准确度、回收率和基质效应 (%)
Tab. 4
| 化合物 | 浓度/(pg·mm-1) | 日内(n=6) | 日间(n=24) | 基质效应 (n=6) | 提取回收率 (n=6) | ||
|---|---|---|---|---|---|---|---|
| 精密度 | 准确度 | 精密度 | 准确度 | ||||
| 苯丙胺 | 5 | 5.7 | 92.5 | 6.2 | 94.8 | 90.1 | 88.2 |
| 250 | 6.7 | 92.0 | 8.1 | 94.3 | 89.0 | 87.6 | |
| 甲基苯丙胺 | 20 | 7.8 | 97.5 | 12.6 | 91.3 | 85.0 | 92.5 |
| 250 | 4.7 | 90.9 | 12.2 | 94.1 | 93.8 | 85.3 | |
| 氯胺酮 | 10 | 2.9 | 92.7 | 8.1 | 91.6 | 80.4 | 90.7 |
| 250 | 3.0 | 91.7 | 6.5 | 95.1 | 86.3 | 84.5 | |
| 吗啡 | 20 | 9.8 | 87.7 | 9.4 | 91.6 | 88.1 | 76.3 |
| 250 | 2.3 | 91.0 | 5.4 | 92.6 | 89.2 | 83.2 | |
| O6-单乙酰吗啡 | 20 | 3.4 | 92.3 | 5.9 | 104.2 | 91.5 | 83.6 |
| 250 | 3.9 | 93.5 | 8.4 | 92.2 | 87.6 | 77.2 | |
| 可卡因 | 5 | 4.9 | 94.5 | 7.6 | 99.2 | 90.2 | 84.1 |
| 250 | 3.9 | 97.2 | 6.1 | 105.3 | 92.4 | 79.2 | |
| 苯甲酰爱康宁 | 2 | 4.0 | 93.4 | 5.3 | 94.8 | 93.4 | 91.2 |
| 250 | 2.9 | 99.5 | 4.2 | 98.0 | 94.5 | 90.8 | |
| 麦角二乙胺 | 1 | 6.1 | 102.1 | 8.8 | 105.2 | 87.2 | 80.5 |
| 250 | 4.9 | 96.7 | 6.4 | 102.2 | 86.4 | 76.5 | |
| 芬太尼 | 20 | 5.2 | 92.0 | 9.4 | 89.5 | 71.3 | 79.2 |
| 250 | 7.9 | 90.5 | 11.2 | 94.5 | 85.4 | 76.2 | |
| 地芬尼多 | 10 | 5.0 | 95.1 | 3.1 | 92.1 | 89.4 | 85.4 |
| 250 | 4.1 | 94.3 | 9.4 | 91.5 | 80.6 | 76.2 | |
| 氟硝西泮 | 2 | 2.4 | 101.9 | 5.3 | 109.2 | 95.4 | 90.6 |
| 250 | 5.1 | 97.6 | 6.9 | 96.1 | 95.6 | 91.2 | |
| 7-氨基氟硝西泮 | 2 | 3.9 | 97.1 | 10.5 | 94.7 | 94.5 | 90.6 |
| 250 | 4.5 | 93.6 | 5.8 | 97.5 | 98.2 | 92.4 | |
| 三唑仑 | 1 | 3.9 | 102.9 | 8.2 | 109.1 | 86.3 | 88.6 |
| 250 | 8.4 | 101.3 | 10.8 | 106.8 | 94.3 | 91.5 | |
| α-羟基三唑仑 | 5 | 7.1 | 96.1 | 11.2 | 93.9 | 88.5 | 76.2 |
| 250 | 6.9 | 97.4 | 10.6 | 95.1 | 85.1 | 78.5 | |
| 可待因 | 20 | 7.9 | 94.9 | 7.9 | 88.2 | 81.2 | 73.5 |
| 250 | 10.2 | 98.4 | 4.9 | 99.2 | 84.9 | 80.2 | |
| 地西泮 | 1 | 8.1 | 98.3 | 11.5 | 100.5 | 89.5 | 88.2 |
| 250 | 6.1 | 102.6 | 8.3 | 104.9 | 92.1 | 91.3 | |
| 去甲地西泮 | 5 | 4.2 | 98.3 | 9.2 | 95.1 | 90.1 | 74.2 |
| 250 | 5.7 | 92.3 | 8.0 | 106.0 | 85.9 | 89.6 | |
| 替马西泮 | 10 | 3.8 | 97.4 | 5.2 | 98.1 | 97.2 | 86.1 |
| 250 | 2.4 | 92.1 | 4.5 | 104.5 | 94.1 | 88.8 | |
| 奥沙西泮 | 20 | 5.1 | 103.5 | 12.7 | 103.6 | 94.5 | 91.6 |
| 250 | 11.8 | 96.8 | 10.2 | 90.4 | 95.6 | 84.5 | |
| 阿普唑仑 | 2 | 5.1 | 98.1 | 7.7 | 96.6 | 88.5 | 76.9 |
| 250 | 4.0 | 97.0 | 6.5 | 98.6 | 84.6 | 77.9 | |
| α-羟基阿普唑仑 | 10 | 8.2 | 95.0 | 11.6 | 90.5 | 85.9 | 88.6 |
| 250 | 6.9 | 93.1 | 10.5 | 94.2 | 89.2 | 79.9 | |
| 氯硝西泮 | 5 | 3.2 | 97.2 | 6.8 | 96.6 | 94.5 | 90.6 |
| 250 | 4.0 | 96.1 | 5.5 | 93.7 | 92.1 | 89.7 | |
| 7-氨基氯硝西泮 | 2 | 4.9 | 93.5 | 5.6 | 96.2 | 94.2 | 94.9 |
| 250 | 5.1 | 94.6 | 9.1 | 96.8 | 96.2 | 89.8 | |
| 艾司唑仑 | 1 | 1.5 | 95.1 | 5.3 | 98.6 | 102.4 | 92.5 |
| 250 | 3.9 | 94.2 | 5.6 | 100.9 | 100.8 | 91.8 | |
| 劳拉西泮 | 20 | 2.1 | 88.4 | 5.6 | 104.6 | 105.2 | 98.2 |
| 250 | 5.1 | 90.6 | 9.4 | 106.6 | 101.5 | 91.5 | |
| 咪达唑仑 | 1 | 4.9 | 97.3 | 7.1 | 94.8 | 98.2 | 92.5 |
| 250 | 2.7 | 100.9 | 8.5 | 97.7 | 103.5 | 86.9 | |
| 硝西泮 | 5 | 4.8 | 97.5 | 9.4 | 93.2 | 109.3 | 89.9 |
| 250 | 5.1 | 90.1 | 8.1 | 103.2 | 107.6 | 84.5 | |
| 7-氨基硝西泮 | 10 | 4.1 | 105.7 | 9.4 | 98.5 | 99.6 | 88.8 |
| 250 | 2.9 | 94.5 | 6.9 | 91.4 | 97.2 | 76.0 | |
| 唑吡坦 | 0.5 | 4.2 | 99.2 | 6.7 | 95.4 | 102.1 | 89.0 |
| 250 | 2.9 | 100.6 | 5.4 | 99.3 | 97.8 | 84.9 | |
| 西酞普兰 | 2 | 4.9 | 98.5 | 5.9 | 105.3 | 94.2 | 86.9 |
| 250 | 7.3 | 96.3 | 8.4 | 96.2 | 98.7 | 83.1 | |
| 苯海拉明 | 2 | 4.5 | 102.4 | 6.3 | 108.6 | 89.4 | 81.1 |
| 250 | 5.2 | 94.2 | 6.9 | 102.1 | 94.2 | 76.2 | |
| 右美沙芬 | 10 | 3.6 | 97.5 | 7.5 | 98.0 | 86.5 | 81.9 |
| 250 | 5.1 | 93.2 | 8.4 | 106.7 | 87.2 | 77.8 | |
| 氯氮平 | 2 | 1.9 | 98.2 | 6.0 | 99.4 | 91.6 | 87.2 |
| 250 | 4.2 | 97.2 | 5.5 | 93.8 | 94.2 | 81.7 | |
| 东莨菪碱 | 0.5 | 2.9 | 86.7 | 5.4 | 92.1 | 89.4 | 86.2 |
| 250 | 8.4 | 104.9 | 10.5 | 106.0 | 102.8 | 82.4 | |
| 右美托咪定 | 5 | 4.6 | 98.1 | 11.2 | 97.2 | 91.5 | 71.5 |
| 250 | 3.5 | 96.2 | 5.6 | 93.4 | 87.5 | 79.1 | |
| 曲马多 | 20 | 9.4 | 91.5 | 6.9 | 105.2 | 94.2 | 68.1 |
| 250 | 2.7 | 94.5 | 3.9 | 93.6 | 88.5 | 71.1 | |
| 安替比林 | 20 | 4.9 | 86.5 | 7.5 | 103.6 | 105.4 | 84.3 |
| 250 | 1.8 | 90.5 | 2.8 | 94.5 | 94.1 | 88.4 | |
| 卡马西平 | 5 | 2.1 | 98.4 | 5.7 | 97.9 | 102.7 | 75.4 |
| 250 | 3.8 | 98.2 | 7.8 | 96.3 | 97.5 | 82.6 | |
| 奥卡西平 | 10 | 3.6 | 97.1 | 9.3 | 96.5 | 100.2 | 89.4 |
| 250 | 4.2 | 102.9 | 6.5 | 100.1 | 104.6 | 79.2 | |
| 尼美西泮 | 2 | 5.1 | 98.2 | 8.8 | 96.8 | 88.9 | 87.2 |
| 250 | 4.6 | 101.7 | 6.7 | 105.5 | 89.4 | 84.9 | |
| 喹硫平 | 2 | 1.7 | 98.2 | 6.0 | 101.8 | 102.7 | 94.2 |
| 250 | 2.0 | 97.2 | 7.4 | 101.7 | 103.8 | 90.8 | |
| 米氮平 | 0.5 | 1.9 | 98.3 | 3.1 | 97.2 | 111.7 | 86.4 |
| 250 | 2.3 | 103.2 | 9.7 | 103.5 | 102.7 | 91.6 | |
2.2.4 提取回收率和基质效应
本研究中各化合物的提取回收率为68.1%~98.2%,基质效应为71.3%~111.7%,详见表4。
2.3 案例应用
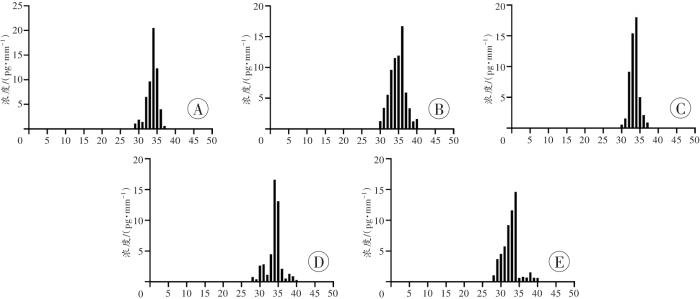
运用本研究方法对单次服用1片唑吡坦(含10 mg酒石酸唑吡坦/片) 28 d后的志愿者单根头发(实验样本)进行分析。结果显示,5根头发中唑吡坦的检出位置位于S28~S40(近根端1.08~1.60 cm),浓度范围为0.62~20.5 pg/mm。单根头发中唑吡坦的总含量为47.2~72.1 pg,平均含量为56.9 pg(n=5),这一结果与之前的报道接近。SHIMA等[22]对单次服用10 mg酒石酸唑吡坦后35 d的黑色头发进行分析,发现单根头发中含有的药物总含量范围为27~63 pg,平均含量为43 pg(n=14)。本例5根头发中4根的峰值浓度出现在S34(近根端1.36 cm),1根头发的峰值浓度出现在S36(近根端1.44 cm),详见图2。根据已知的服药时间计算可知,该志愿者的头发生长速度为0.49~0.51 mm/d,约为1.5 cm/月,比通常认为的1 cm/月要快。因此,不同个体的头发生长速度存在差异。在药物辅助犯罪案件中,需要以个体本身头发的生长速度进行推算,以提高药物摄入时间估计的准确性。
图2
图2
唑吡坦在5根头发中的分布
A~E分别为5根头发中唑吡坦的分布,横坐标表示头发片段。
Fig. 2
Distribution of zolpidem in 5 hairs
3 结 论
本研究建立了0.4 mm头发片段中42种精神活性物质的LC-MS/MS定性定量分析方法,并成功应用于单次服用唑吡坦的志愿者头发样本的分析,在5根头发中均检出唑吡坦,表明头发微分段分析技术可用于唑吡坦单次摄药案件的检测。然而,同一个体的头发间可能处于不同的生长阶段[23],在对案件结果进行分析和评价时,需要尽量基于多根头发的分析结果以排除操作误差及偶然性。此外,未来还需要将微分段分析技术应用于涉及更多药物的案例中,以进一步证明单根头发微分段分析技术在DFSA案件中的可行性。
参考文献
头发中氯硝西泮的分段分析在药物辅助犯罪案件中的作用
[J].
The role of segmental analysis of clonazepam in hair in drug facilitated cases
[J].
Hair analysis for drug detection
[J].
Segmental hair analysis using liquid chromatography-tandem mass spectrometry after a single dose of benzodia-zepines
[J].
Hair analysis by liquid chromatography-tandem mass spectrometry in toxicological investigation of drug-facilitated crimes: Report of 128 cases over the period June 2003-May 2004 in metropolitan Paris
[J].
Incorporation of five common hypnotics into hair after a single dose and application to a forensic case of drug facilitated crimes
[J].
The use of hair as a toxicological tool in DFC casework
[J].
Guidelines for collection of biological samples for clinical and forensic toxicological analysis
[J].
Segmental analysis of antidepressant and antipsychotic drugs in the hair of schizophrenic patients
[J].
Segmental hair analysis and estimation of methamphetamine use pattern
[J].
Determination of antidepressants in hair via UHPLC-MS/MS as a complementary informative tool for clinical and forensic toxicological assessments
[J].
Development of an improved method to estimate the days of continuous drug ingestion, based on the micro-segmental hair analysis
[J].
Two DFSA cases involving midazolam clarified by the micro-segmental hair analyses
[J].
质谱成像技术及其在法医毒理学中的应用
[J].
Mass spectrometry imaging and its application in forensic toxicology
[J].
Relationship between methamphetamine use history and segmental hair analysis findings of MA users
[J].
Determination of cocaine, cocaine metabolites and cannabinoids in single hairs by MALDI Fourier transform mass spectrometry -- Preliminary results
[J].
Single hair analysis of small molecules using MALDI-triple quadrupole MS imaging and LC-MS/MS: Investigations on opportunities and pitfalls
[J].
Hair analysis in clinical and forensic toxicology
[J].
生物样品分析方法的有效性验证
[J].
How to validate a bio-analytical method
[J].
Strategies for the assessment of matrix effect in quantitative bioanalytical methods based on HPLC-MS/MS
[J].
Different localizations of drugs simultaneously administered in a strand of hair by micro-segmental analysis
[J].
Single hair analysis: Validation of a screening method for over 150 analytes and application on documented single-dose cases
[J].
Single-hair analysis of zolpidem on the supposition of its single administration in drug-facilitated crimes
[J].
Hair testing for drugs of abuse and new psychoactive substances in a high-risk population
[J].